15838214737
企业办理ISO13485医疗器械管理体系认证的条件是什么?
最近几年有越来越多的公司申请了ISO体系认证,于是没有申请过ISO体系认证的公司也有想法要申请,因此很想要申请ISO13485医疗器械管理体系认证,但之前并没有申请过ISO体系认证,对ISO13485医疗器械管理体系认证的了解并不多,于是就想要知道企业办理ISO13485医疗器械管理体系认证的条件是什么?下面就跟小编一起去看看吧。

申请质量管理体系认证注册条件:
1申请组织应持有法人营业执照或证明其法律地位的文件。
2已取得生产许可证或其它资质证明(国家或部门法规有要求时);
3申请认证的质量管理体系覆盖的产品应符合有关国家标准、行业标准或注册产品标准(企业标准),产品定型且成批生产。
4申请组织应建立符合拟申请认证标准的管理体系、对医疗器械生产、经营企业还应符合YY/T0287标准的要求,生产三类医疗器械的企业,质量管理体系运行时间不少于6个月,生产和经营其它产品的企业,质量管理体系运行时间不少于3个月。并至少进行过一次全面内部审核及一次管理评审。
5在提出认证申请前的一年内,申请组织的产品无重大顾客投诉及质量事故。
 相关推荐
相关推荐-
ISO13485医疗器械管理体系认证申请的条件有哪些?

一、申请人应具有明确的法律地位 二、申请人应具备相应的许可资质 1、对于生产型企业,I类产品需提供医疗器械产品备案凭证

 热门阅读
热门阅读-
什么是FEMA(潜在失效模式与后果分析)
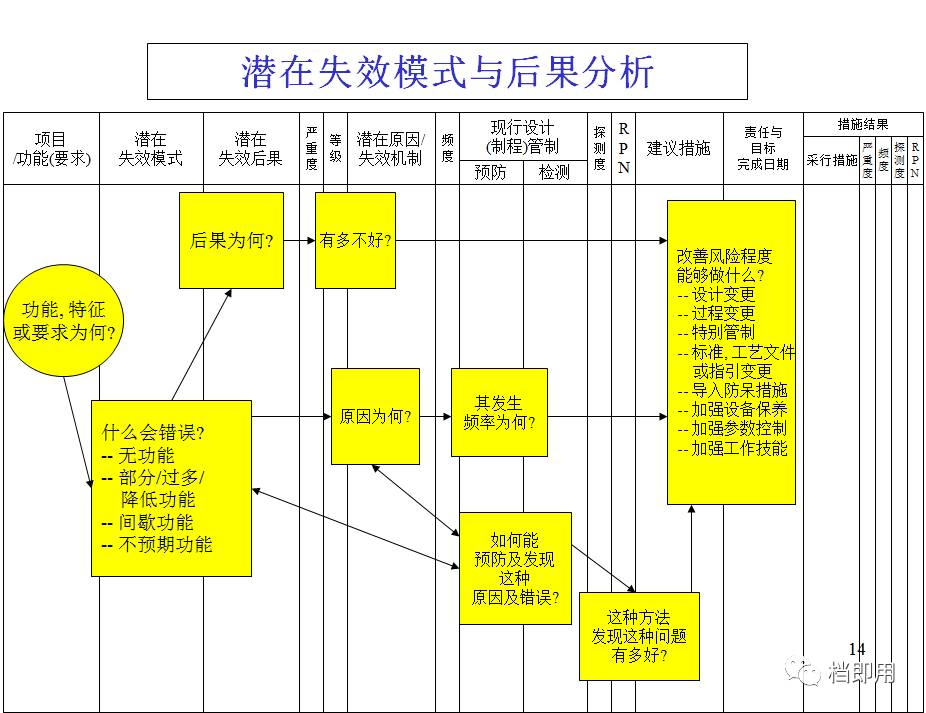
FMEA是失效模式与影响分析的缩写,因其英文名称时Failure Mode and Effects Analysis,所以简写为FMEA,也就是潜在失效模式与后果分析,FME
-
三体系认证每年都要审核么

三体认证的有效期为三年,并且每年都要进行监督审核。ISO三体系认证三年需要审核三次,首次初审,其余两次是监审,也就是监督
-
DAkkS是什么意思?DAkkS的职责是什么

DAKKS是什么?DAkks德国认可委员会认可的实验室资质,它相当于德国的认监委,在大约4300个认证程序中,DAkkS作为一个独立机构,评估和
-
职业危害因素的来源分为哪几种?

物理因素 主要为异常气象条件如高温、高湿、低温等;异常气压如高气压、低气压等;噪声及振动;非电离辐射如可见光、紫外线、红外
-
粉尘爆炸有哪五个条件?

粉尘爆炸的五个条件 一、空气(氧气); 二、浓度超过MEC的可燃性干粉尘; 三、点火源; 四、空间受限或封闭; 五、分成悬浮、分散(与氧
 最新文章
最新文章-
 认证知识 2023-04-18
认证知识 2023-04-18 -
 认证知识 2023-04-18
认证知识 2023-04-18 -
 认证知识 2023-04-18
认证知识 2023-04-18 -
 认证知识 2023-04-18
认证知识 2023-04-18 -
 认证知识 2023-04-18
认证知识 2023-04-18
